-
![[image]](https://www.balancer.ru/cache/sites/net/tw/twirpx/cv01/0122/128x128-crop/0122290.jpg)
Синтез хлоратов и перхлоратов
Теги:
RLAN> Я три месяца маюсь что бы найти наилучший способ получения дистилированной воды.
Это просто в нашей части мира - вот многоцелевой инструмент, всегда есть знакомы у которого есть один
Или сделай себе один из старого нержавеющего горшка, ведро и некоторый шланг.
Это просто в нашей части мира - вот многоцелевой инструмент, всегда есть знакомы у которого есть один

Или сделай себе один из старого нержавеющего горшка, ведро и некоторый шланг.


Это сообщение редактировалось 11.03.2017 в 11:47
Посуда:
Тазик (на случай разлива), тряпка (прокладка), 3-литровая стеклобанка.
Или банка в раковине, чтоб сразу всё в канализацию утекло при аварии.
У меня банки внезапное наливание кипятка держат, из сотен наливаний ни разу не. Но надо смотреть, чтоб не было трещин и дефектов.
Порции бОльшие, чем 3 л не делал, неудобно.
Нельзя раствор в банке размешивать металлической ложкой, только пластиковой или деревянной (палкой). После нескольких десятков лёгких ударов ложкой о стекло банка обязательно треснет.
При смешении концентрированных кислот и щелочей нагрев почти всегда приводит к вскипанию.
Надо это делать в большом количестве нейтральной жидкости.
Наверное надо начать со 100 граммов воды, прилить туда 20 мл аммиака (вонять всё равно будет сильно), а потом прилить 25 мл кислоты.
Или в обратном порядке, чтоб меньше вони.
Нейтрализовать, учитывая добавляемое количество, чтоб на будущее знать точно, в каком именно отношении надо смешивать аммиак и кислоту.
Лакмусовой бумажкой тыкать, или её чем-то.
Можно, кстати, чуть фенолфталеина добавить, чтоб сразу было видно.
И посмотреть, насколько это нагреется. Чтоб на будущее знать, сколько можно в балластный раствор добавлять аммиака с кислотой.
Ну, чтоб не перегреть до вскипания, но чтоб температура была высокой и ПХА полностью растворялся.
И так вначале понемногу добавлять, пока объём раствора не дойдёт литров до 2 ... 2.5.
Это и тренировка будет хорошая.
Потом дать раствору охладиться для выпадения кристаллов, и потом ещё в холодильнике охладить (не обязательно).
А потом слитый раствор опять использовать как буфер для смешения аммиака и кислоты.
Количество раствора будет расти, так что воду из него надо будет или упаривать, или вымораживать.
Упаривать нейтрализованный раствор ПХА вполне можно в эмалированном тазике, не пострадает.
В тазике поверхность раствора большая для лучшего испарения.
Но не надо доводить до кипения с бульканьем — когда пузырьки лопаются на поверхности. Пусть они у дна появляются и там же исчезают. Иначе всё вокруг будет в брызгах.
Помешивание сильно интенсифицирует испарение и уменьшает бульканье.
Если вымораживать, то можно морозить в пластиковой бутылке,
Когда получится ещё подвижная каша, вываливать её в удобную посуду и оттуда выгребать лёд на тряпичный фильтр.
То, что стекает — обратно в раствор, а на фильтре останется почти чистый лёд.
Не надо забывать, что при замерзании объём увеличивается — чтоб бутылка не лопнула в морозильнике.
Тазик (на случай разлива), тряпка (прокладка), 3-литровая стеклобанка.
Или банка в раковине, чтоб сразу всё в канализацию утекло при аварии.
У меня банки внезапное наливание кипятка держат, из сотен наливаний ни разу не. Но надо смотреть, чтоб не было трещин и дефектов.
Порции бОльшие, чем 3 л не делал, неудобно.
Нельзя раствор в банке размешивать металлической ложкой, только пластиковой или деревянной (палкой). После нескольких десятков лёгких ударов ложкой о стекло банка обязательно треснет.
При смешении концентрированных кислот и щелочей нагрев почти всегда приводит к вскипанию.
Надо это делать в большом количестве нейтральной жидкости.
Наверное надо начать со 100 граммов воды, прилить туда 20 мл аммиака (вонять всё равно будет сильно), а потом прилить 25 мл кислоты.
Или в обратном порядке, чтоб меньше вони.
Нейтрализовать, учитывая добавляемое количество, чтоб на будущее знать точно, в каком именно отношении надо смешивать аммиак и кислоту.
Лакмусовой бумажкой тыкать, или её чем-то.
Можно, кстати, чуть фенолфталеина добавить, чтоб сразу было видно.
И посмотреть, насколько это нагреется. Чтоб на будущее знать, сколько можно в балластный раствор добавлять аммиака с кислотой.
Ну, чтоб не перегреть до вскипания, но чтоб температура была высокой и ПХА полностью растворялся.
И так вначале понемногу добавлять, пока объём раствора не дойдёт литров до 2 ... 2.5.
Это и тренировка будет хорошая.
Потом дать раствору охладиться для выпадения кристаллов, и потом ещё в холодильнике охладить (не обязательно).
А потом слитый раствор опять использовать как буфер для смешения аммиака и кислоты.
Количество раствора будет расти, так что воду из него надо будет или упаривать, или вымораживать.
Упаривать нейтрализованный раствор ПХА вполне можно в эмалированном тазике, не пострадает.
В тазике поверхность раствора большая для лучшего испарения.
Но не надо доводить до кипения с бульканьем — когда пузырьки лопаются на поверхности. Пусть они у дна появляются и там же исчезают. Иначе всё вокруг будет в брызгах.
Помешивание сильно интенсифицирует испарение и уменьшает бульканье.
Если вымораживать, то можно морозить в пластиковой бутылке,
Когда получится ещё подвижная каша, вываливать её в удобную посуду и оттуда выгребать лёд на тряпичный фильтр.
То, что стекает — обратно в раствор, а на фильтре останется почти чистый лёд.
Не надо забывать, что при замерзании объём увеличивается — чтоб бутылка не лопнула в морозильнике.


Это сообщение редактировалось 11.03.2017 в 12:05
Xan> Лакмусовой бумажкой тыкать, или её чем-то.
аммиак - слабое основание, поэтому эквимолярный раствор имеет кислую реакцию.
Xan> Можно, кстати, чуть фенолфталеина добавить, чтоб сразу было видно.
не, лучше не надо. лучше пусть будет избыток аммиака, чем свободной хлорной кислоты.
аммиак - слабое основание, поэтому эквимолярный раствор имеет кислую реакцию.
Xan> Можно, кстати, чуть фенолфталеина добавить, чтоб сразу было видно.
не, лучше не надо. лучше пусть будет избыток аммиака, чем свободной хлорной кислоты.


Xan>> Можно, кстати, чуть фенолфталеина добавить, чтоб сразу было видно.
Б.г.> не, лучше не надо. лучше пусть будет избыток аммиака, чем свободной хлорной кислоты.
Я тут по случаю прикупил детский pH-метр, всего за двадцать баксов.
А то в хим лабазе только за электрод больше стольника ломили!
Сделал раствор ПХА, 10 ... 20% — на глаз щепотку сыпанул.
pH = 6.2
Так что для покраснения пургена надо как раз ещё аммиака лишнего добавлять. Он краснеет при pH > 8.2.
Всё в порядке.
Б.г.> не, лучше не надо. лучше пусть будет избыток аммиака, чем свободной хлорной кислоты.
Я тут по случаю прикупил детский pH-метр, всего за двадцать баксов.
А то в хим лабазе только за электрод больше стольника ломили!

Сделал раствор ПХА, 10 ... 20% — на глаз щепотку сыпанул.
pH = 6.2
Так что для покраснения пургена надо как раз ещё аммиака лишнего добавлять. Он краснеет при pH > 8.2.
Всё в порядке.


Xan> Сделал раствор ПХА, 10 ... 20% — на глаз щепотку сыпанул.
Xan> pH = 6.2
Xan> Так что для покраснения пургена надо как раз ещё аммиака лишнего добавлять. Он краснеет при pH > 8.2.
Вопрос в том, СКОЛЬКО аммиака надо долить это ж буферная система получается, классика, слабое основание + сильная кислота.
это ж буферная система получается, классика, слабое основание + сильная кислота.
Xan> pH = 6.2
Xan> Так что для покраснения пургена надо как раз ещё аммиака лишнего добавлять. Он краснеет при pH > 8.2.
Вопрос в том, СКОЛЬКО аммиака надо долить
 это ж буферная система получается, классика, слабое основание + сильная кислота.
это ж буферная система получается, классика, слабое основание + сильная кислота.


Спасибо за подсказки.
Лакмусовые полоски у меня есть, пургена нет
Купить не сложно, а надо?
Уж больно плотный график у меня последнее время. Десять дней. И другие дела никто не отменял.
Потом снова солнечная Грузия на непонятный срок.
Поэтому и пытаюсь заранее понять, что я должен сделать/купить, и что смогу успеть.
Лакмусовые полоски у меня есть, пургена нет

Купить не сложно, а надо?
Уж больно плотный график у меня последнее время. Десять дней. И другие дела никто не отменял.
Потом снова солнечная Грузия на непонятный срок.
Поэтому и пытаюсь заранее понять, что я должен сделать/купить, и что смогу успеть.


"Накося выкуси".
Сижу и выкусываю контакты из релюшек. Должно набраться больше 3 грамм ПлИ-10. Неожиданно геморройным оказалось вскрытие РЭС-10. В детстве, помнится, вскрывал их без напряжения. Хочется сегодня всё доделать и уже протравить остатки латуни и бронзы...
Вот только потом чем переплавлять? нужна же кислород-водородная горелка. Или можно кислород-пропановой с избытком кислорода?
Сижу и выкусываю контакты из релюшек. Должно набраться больше 3 грамм ПлИ-10. Неожиданно геморройным оказалось вскрытие РЭС-10. В детстве, помнится, вскрывал их без напряжения. Хочется сегодня всё доделать и уже протравить остатки латуни и бронзы...
Вот только потом чем переплавлять? нужна же кислород-водородная горелка. Или можно кислород-пропановой с избытком кислорода?


Б.г.> Вот только потом чем переплавлять? нужна же кислород-водородная горелка. Или можно кислород-пропановой с избытком кислорода?
Любая с кислородом даст нужную температуру.
С избытком кислорода тоже всё понятно.
Собсна — "не коптящее" достаточно.
Как я понимаю, будешь через химию прогонять, чтоб чистую получить, а не сплав?
Любая с кислородом даст нужную температуру.
С избытком кислорода тоже всё понятно.
Собсна — "не коптящее" достаточно.
Как я понимаю, будешь через химию прогонять, чтоб чистую получить, а не сплав?


ПХА в этиловом спирте, вроде бы, растворяется. Чем его лучше смачивать при помоле, изопропиловым?


Б.г.>> Вот только потом чем переплавлять? нужна же кислород-водородная горелка. Или можно кислород-пропановой с избытком кислорода?
Xan> Любая с кислородом даст нужную температуру.
На самом деле, нет. Я плавил свою платину много раз, пока не усвоил технологию для прокатки и плавки. Если едва расплавит платины, она не будет отделять оксиды. Действительно нужная водород или ацетилен (МАП)-кислородная горелка чтобы расплавить и/или испарить все оксиды, иначе они останутся в кристаллической структуре.
Платина плавится при 1800o а температура пропан-кислородная горелка 2200o в лучшем случае - разница слишком мала и она не достаточно вискозная.
Также если температура в жидкой фазе недостаточно высока, когда она остывает она не образует правильной кристаллической структуры и становится с высокими размерами зерен. Такой расплавленный слиток становится очень хрупким и не может коватся.
Хорошим показателем при плавлении является яркость. Сначала платина плавится и образует каплю, капля становится ярче и ярче белая. Если продолжим еe нагрев то в данной моменте она становится из белая немного красно-желтой, а яркость заметно падает, вязкость тоже - вот что нам нужно.
Первые 5-6 раз, чтобы сэкономить на кислороде я не пошел в эту точку и имел массу проблем. После нескольких случайних перегревов платины я заметил эти эффекты и заметное улучшение в ковкости (прокатке) - поэтому я начал экспериментировать.
Xan> Любая с кислородом даст нужную температуру.
На самом деле, нет. Я плавил свою платину много раз, пока не усвоил технологию для прокатки и плавки. Если едва расплавит платины, она не будет отделять оксиды. Действительно нужная водород или ацетилен (МАП)-кислородная горелка чтобы расплавить и/или испарить все оксиды, иначе они останутся в кристаллической структуре.
Платина плавится при 1800o а температура пропан-кислородная горелка 2200o в лучшем случае - разница слишком мала и она не достаточно вискозная.
Также если температура в жидкой фазе недостаточно высока, когда она остывает она не образует правильной кристаллической структуры и становится с высокими размерами зерен. Такой расплавленный слиток становится очень хрупким и не может коватся.
Хорошим показателем при плавлении является яркость. Сначала платина плавится и образует каплю, капля становится ярче и ярче белая. Если продолжим еe нагрев то в данной моменте она становится из белая немного красно-желтой, а яркость заметно падает, вязкость тоже - вот что нам нужно.
Первые 5-6 раз, чтобы сэкономить на кислороде я не пошел в эту точку и имел массу проблем. После нескольких случайних перегревов платины я заметил эти эффекты и заметное улучшение в ковкости (прокатке) - поэтому я начал экспериментировать.


Massaraksh> ПХА в этиловом спирте, вроде бы, растворяется. Чем его лучше смачивать при помоле, изопропиловым?
Горючую органику лучше не использовать. Мне кажется!
Нерастворяющие жидкости, например:
(способ получения перхлората аммония - патент РФ 2246472 - Куценко Г.В. ,Колосов Г.Г. ,Чернов М.А. ,Шабаев Г.И. ,Хлюпина В.А. ,Божья-Воля Н.С. ,Тудвасев В.И.)
"трифтортрихлорэтана, хлористого метилена"
Но на мой взгляд лучшей и безопасной жидкостью является насыщенный раствор ПХА в воде.
А в нескольких патентах заметил, что любят при размоле добавлять лецитин. Как ПАВ.
Надо будет попробовать.
Горючую органику лучше не использовать. Мне кажется!

Нерастворяющие жидкости, например:
(способ получения перхлората аммония - патент РФ 2246472 - Куценко Г.В. ,Колосов Г.Г. ,Чернов М.А. ,Шабаев Г.И. ,Хлюпина В.А. ,Божья-Воля Н.С. ,Тудвасев В.И.)
"трифтортрихлорэтана, хлористого метилена"
Но на мой взгляд лучшей и безопасной жидкостью является насыщенный раствор ПХА в воде.

А в нескольких патентах заметил, что любят при размоле добавлять лецитин. Как ПАВ.
Надо будет попробовать.


Xan> Как я понимаю, будешь через химию прогонять, чтоб чистую получить, а не сплав?
Да вот опять заколебался, панимаиш Разные источники противоречат друг другу, может, и ПлИ-10 будет нормально работать. Хотя сопротивление у него больше, чем у чистой платины. а у неё и так немаленькое.
Разные источники противоречат друг другу, может, и ПлИ-10 будет нормально работать. Хотя сопротивление у него больше, чем у чистой платины. а у неё и так немаленькое.
Да вот опять заколебался, панимаиш
 Разные источники противоречат друг другу, может, и ПлИ-10 будет нормально работать. Хотя сопротивление у него больше, чем у чистой платины. а у неё и так немаленькое.
Разные источники противоречат друг другу, может, и ПлИ-10 будет нормально работать. Хотя сопротивление у него больше, чем у чистой платины. а у неё и так немаленькое.


Xan>> Как я понимаю, будешь через химию прогонять, чтоб чистую получить, а не сплав?
Б.г.> Да вот опять заколебался, панимаиш Разные источники противоречат друг другу, может, и ПлИ-10 будет нормально работать. Хотя сопротивление у него больше, чем у чистой платины. а у неё и так немаленькое.
Разные источники противоречат друг другу, может, и ПлИ-10 будет нормально работать. Хотя сопротивление у него больше, чем у чистой платины. а у неё и так немаленькое.
Почитал ещё.
Похоже, для хлоратов сплав лучше.
А про перхлораты не увидел.
Но механически сплав более жёсткий. И сопротивление больше, да.
А чистая — проверенное дело. Но химия нужна.
"По три, но маленькие, большие, но по пять!"
Или вот так:
"Решения, решения..."
(https://dl.dropboxusercontent.com/u/6706516/Postal.mp4)
Осторожно, в ролике звучат нехорошие слова!
Б.г.> Да вот опять заколебался, панимаиш
 Разные источники противоречат друг другу, может, и ПлИ-10 будет нормально работать. Хотя сопротивление у него больше, чем у чистой платины. а у неё и так немаленькое.
Разные источники противоречат друг другу, может, и ПлИ-10 будет нормально работать. Хотя сопротивление у него больше, чем у чистой платины. а у неё и так немаленькое.Почитал ещё.
Похоже, для хлоратов сплав лучше.
А про перхлораты не увидел.
Но механически сплав более жёсткий. И сопротивление больше, да.
А чистая — проверенное дело. Но химия нужна.
"По три, но маленькие, большие, но по пять!"
Или вот так:
"Решения, решения..."
(https://dl.dropboxusercontent.com/u/6706516/Postal.mp4)
Осторожно, в ролике звучат нехорошие слова!


Привет,
У меня есть следующий вопрос - возникла эта мысль:
- В клетках, с не контролируемых рН >+9 и температура ниже 60 градусов - реакции идет только одним путем (анодного формирование хлората) и теоретический максимальный выход составляет 66%.
- Любые потери ниже от етих 66% обусловлены катодным восстановлением хлоратов.
- Когда используются хроматы, они создают защитную пленку на катодом для уменьшения катодного восстановления хлоратов.
- Но эффект буферизации хроматы в этих количествах пренебрежимо мал - т.е не может понизить его ниже чем 7 чтобы дать возможность другой реакции.
- Титановые катоды не восстанавливают хлораты.
Таким образом, похоже что если мы используем титановые катоды то нет необходимости для хроматах и эффективность должна быть близка к максимально возможной в этих условиях - то есть 66%.
Можно дать совет если я что-то пропустил и имеет ли этих размышления смысл?
У меня есть следующий вопрос - возникла эта мысль:
- В клетках, с не контролируемых рН >+9 и температура ниже 60 градусов - реакции идет только одним путем (анодного формирование хлората) и теоретический максимальный выход составляет 66%.
- Любые потери ниже от етих 66% обусловлены катодным восстановлением хлоратов.
- Когда используются хроматы, они создают защитную пленку на катодом для уменьшения катодного восстановления хлоратов.
- Но эффект буферизации хроматы в этих количествах пренебрежимо мал - т.е не может понизить его ниже чем 7 чтобы дать возможность другой реакции.
- Титановые катоды не восстанавливают хлораты.
Таким образом, похоже что если мы используем титановые катоды то нет необходимости для хроматах и эффективность должна быть близка к максимально возможной в этих условиях - то есть 66%.
Можно дать совет если я что-то пропустил и имеет ли этих размышления смысл?



Б.г.> "Накося выкуси".
Выкусил.
"Всё, нажитое непосильным трудом":
Ну, больше половины этого - неблагородные металлы, которые я стравлю азоткой... Должно остаться чуть больше 3 граммов ПлИ-10.
Выкусил.
"Всё, нажитое непосильным трудом":
Ну, больше половины этого - неблагородные металлы, которые я стравлю азоткой... Должно остаться чуть больше 3 граммов ПлИ-10.
Прикреплённые файлы:


pinko> - В клетках, с не контролируемых рН >+9 и температура ниже 60 градусов - реакции идет только одним путем (анодного формирование хлората) и теоретический максимальный выход составляет 66%.
Откуда такая пессимистическая цифра?
В книжках такого нет.
У меня КПД был больше 90%. Это до перхлората.
pinko> Таким образом, похоже что если мы используем титановые катоды то нет необходимости для хроматах и эффективность должна быть близка к максимально возможной в этих условиях - то есть 66%.
pinko> Можно дать совет если я что-то пропустил и имеет ли этих размышления смысл?
У меня в одной ячейке титановый катод, в другой нихромовый.
Но я не смотрел, где именно какой. Вроде, они одинаково работали по КПД.
В обеих я использовал и хромат и кальций для уменьшения восстановления.
С хроматом без кальция тоже получалось плохо.
Откуда такая пессимистическая цифра?
В книжках такого нет.
У меня КПД был больше 90%. Это до перхлората.
pinko> Таким образом, похоже что если мы используем титановые катоды то нет необходимости для хроматах и эффективность должна быть близка к максимально возможной в этих условиях - то есть 66%.
pinko> Можно дать совет если я что-то пропустил и имеет ли этих размышления смысл?

У меня в одной ячейке титановый катод, в другой нихромовый.
Но я не смотрел, где именно какой. Вроде, они одинаково работали по КПД.
В обеих я использовал и хромат и кальций для уменьшения восстановления.
С хроматом без кальция тоже получалось плохо.


Xan> Откуда такая пессимистическая цифра?
Я взял ее отсюда, они ссылаются на етот источник:

Я взял ее отсюда, они ссылаются на етот источник:
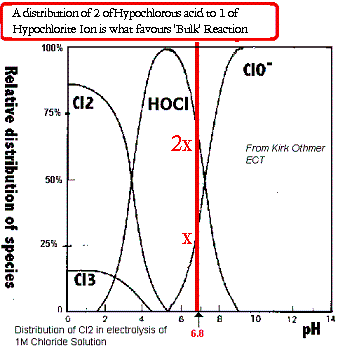
Comprehensive Treatise of Electro chemistry Vol. 2 Electrochemical Processing. J. O. M. Bockris, B. E. Conway, E. Yeager, R. E. White. Plenum Press, N.Y. 1981, also The Kirk-Othmer Encyclopedia of Chemical Tech.

Diagram on left shows the dependency of the concentration of intermediate species in the chlorate cell on pH. At a low pH the cell will generate Chlorine gas which will escape out of the cell and this will cause the pH to increase. As the pH rises the ease with which Chlorine can escape out of the cell gets less and less and the cell will stabilize at a pH of about 9 or 10. At this high pH, practically all Chlorate is made by electricity by the Anodic Oxidation of the Hypochlorous ion (Anodic Chlorate formation) at a maximum possible current efficiency of 66.66%, the nine electron route. Adding acid lowers the pH which will decrease the concentration of the Hypochlorous ion and increase the concentration of the Hypochlorous acid. Thus it will be possible for Chlorate to form in the bulk of the solution by these species combining (Chemical Chlorate formation), the six electron route.



Похоже, что система свинец-висмут-олово, соленая вода и платина образуют некий термит который при достаточном нагреве (но не настолько высоком) начинает самоподдерживающуюся реакцию, которая сжигает платину до пеплом. Честно, это слишком интересно чтобы не исследовать, но связано с сжиганием платины ... что вроде дорого. Я пытался повторить это без платины, но не работает. 
Первый раз я заметил ето, когда отремонтировал с горелку стеклянную ампулу с платиновой проволокой и Розе сплавом внутри, где была утечка соленой воды. Сплав и платина начали расширяться как губка и стали коричнево-черный пепел, включая стекло - не осталось следа платиновой проволоки - она просто исчезла. Тогда я не смог это задокументировать и тоже был скептиком - просто предположил, что я вероятно пропустил тонкую платину.
Два дня назад мой источник питания вышел из строя из-за сильного холода снаружи.И начал работать при напряжении 12В пропуская много ампер через электрод. Это сильно нагревало платину, которая достаточно нагревала клей для локального воспламенения незначительных следов хлоратов/перхлоратов. Это было достаточно, чтобы зажечь термит где был припой (сплав Розе) и ето сжигало на етот раз толстый лист платину до пепел.
Сейчась я сделал фотографии - но не догадываюсь что может сгореть платина в пепел? Любая идея какая реакция была которая разрушает так платину.

Первый раз я заметил ето, когда отремонтировал с горелку стеклянную ампулу с платиновой проволокой и Розе сплавом внутри, где была утечка соленой воды. Сплав и платина начали расширяться как губка и стали коричнево-черный пепел, включая стекло - не осталось следа платиновой проволоки - она просто исчезла. Тогда я не смог это задокументировать и тоже был скептиком - просто предположил, что я вероятно пропустил тонкую платину.
Два дня назад мой источник питания вышел из строя из-за сильного холода снаружи.И начал работать при напряжении 12В пропуская много ампер через электрод. Это сильно нагревало платину, которая достаточно нагревала клей для локального воспламенения незначительных следов хлоратов/перхлоратов. Это было достаточно, чтобы зажечь термит где был припой (сплав Розе) и ето сжигало на етот раз толстый лист платину до пепел.

Сейчась я сделал фотографии - но не догадываюсь что может сгореть платина в пепел? Любая идея какая реакция была которая разрушает так платину.


pinko> Похоже, что система свинец-висмут-олово, соленая вода и платина образуют некий термит который при достаточном нагреве (но не настолько высоком) начинает самоподдерживающуюся реакцию, которая сжигает платину до пеплом.
В расплавленном свинце платина растворяется, со скоростью, примерно, как сахар в чае, намного быстрее, чем в царской водке. Поэтому есть рецепт по хим. очистке платины - сначала платиносодержащие отходы растворяются в свинце, потом сплав травится в чистой азотной кислоте, а потом мелкодисперсный остаток - в царской водке. Так получается намного быстрее, чем травить платину из компактного состояния.
В сплаве Розе, видимо, тоже, как только он расплавился от перегрева. То, что ты зовёшь "пепел" - это смесь оксидов свинца, висмута, и олова, которая приняла форму бывшего платинового электрода. Вся платина, что "ушла", ушла в припой.
В расплавленном свинце платина растворяется, со скоростью, примерно, как сахар в чае, намного быстрее, чем в царской водке. Поэтому есть рецепт по хим. очистке платины - сначала платиносодержащие отходы растворяются в свинце, потом сплав травится в чистой азотной кислоте, а потом мелкодисперсный остаток - в царской водке. Так получается намного быстрее, чем травить платину из компактного состояния.
В сплаве Розе, видимо, тоже, как только он расплавился от перегрева. То, что ты зовёшь "пепел" - это смесь оксидов свинца, висмута, и олова, которая приняла форму бывшего платинового электрода. Вся платина, что "ушла", ушла в припой.


pinko>Любая идея какая реакция была которая разрушает так платину.
А такого не может быть?
А такого не может быть?
Соединения платины с хлором можно получить действием газообразного хлора па платину.
При нормальном давлении и при температуре ниже 370° получается хлористая платина ржаво-коричневого цвета. При температуре 370° она переходит в треххлористую платину черно-зеленого цвета, которая при нагревании до 435° распадается на хлор и двухлористую платину коричнево-зеленого цвета. При дальнейшем нагревании при 582° хлор окончательно теряется, и остается металлическая платина.
Источник: Химические соединения платины


Copyright © Balancer 1997..2022
Создано 17.04.2012
Связь с владельцами и администрацией сайта: anonisimov@gmail.com, rwasp1957@yandex.ru и admin@balancer.ru.
Создано 17.04.2012
Связь с владельцами и администрацией сайта: anonisimov@gmail.com, rwasp1957@yandex.ru и admin@balancer.ru.
 Xan
Xan

 инфо
инфо инструменты
инструменты pinko
pinko


 Бывший генералиссимус
Бывший генералиссимус

 RLAN
RLAN










